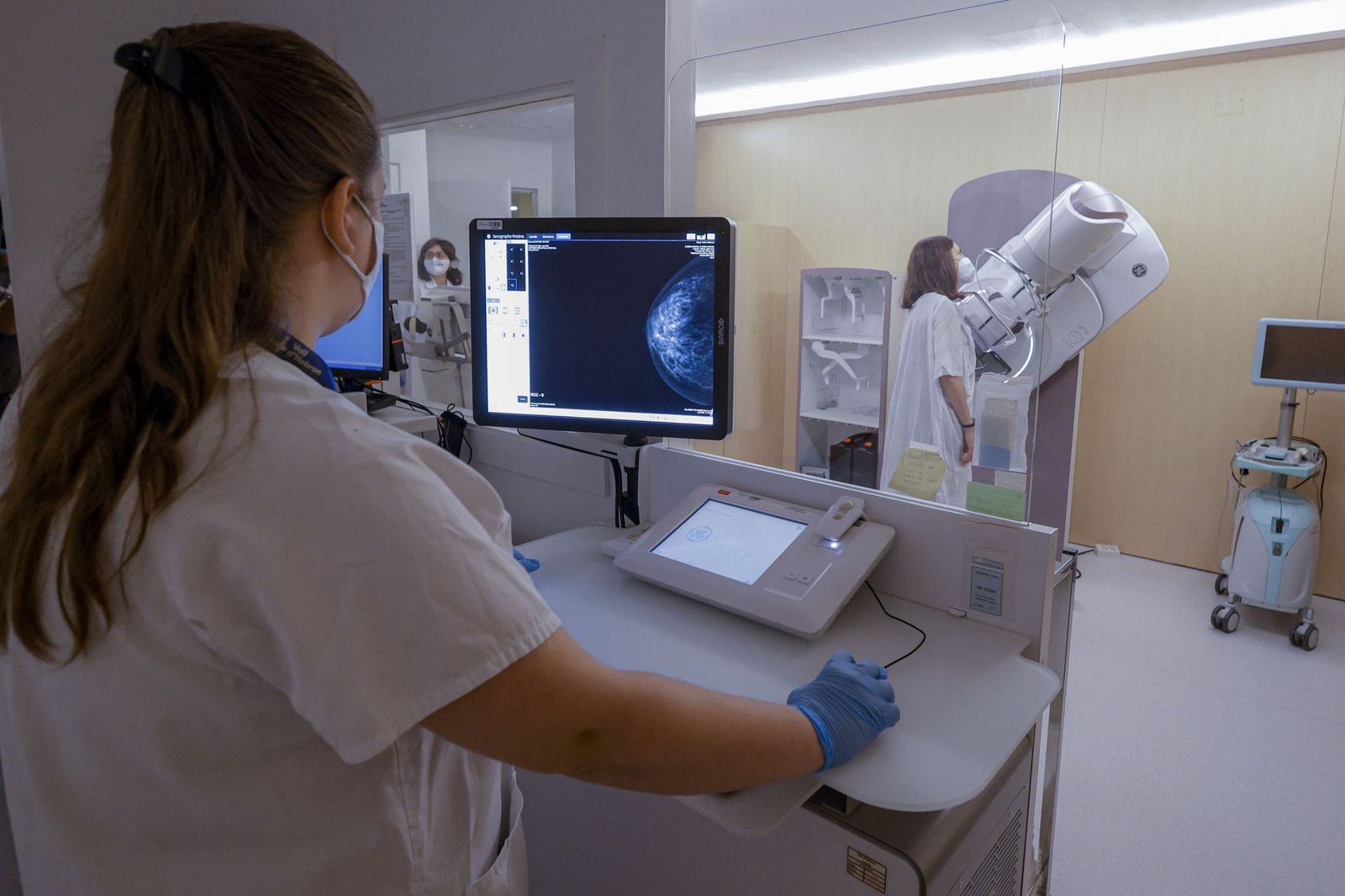
Coronavirus: Dudas sobre la efectividad de la vacuna de Oxford y AstraZeneca
Crisis sanitaria
Tras haber anunciado los resultados preliminares de la tercera fase de las pruebas, la universidad reconoce que a la hora de suministrar las dosis a los participantes de los ensayos se partió de un error
AstraZeneca planea un nuevo estudio para validar su eficacia

La Universidad de Oxford ha admitido que, por equivocación, hubo "diferencias" en la forma de administrar las dosis de su vacuna contra el coronavirus a los voluntarios en los ensayos, pero aclaró que los métodos para medir la concentración del antídoto han quedado ya "establecidos".
En un comunicado, la universidad británica pretende despejar las crecientes dudas surgidas en los últimos días sobre la efectividad de hasta un 90% que se observó en el subgrupo que recibió primero media dosis y después una dosis completa del producto que ha desarrollado con la farmacéutica sueco-británica AstraZeneca.
Un error en las dosis
Tras haber anunciado el pasado día 23 los resultados preliminares de la tercera fase de las pruebas, la universidad reconoce de manera implícita que a la hora de suministrar las dosis a los participantes de los ensayos se partió de un error.
El grupo de expertos, liderado por Andrew Pollard y Sarah Gilbert, informó en un principio de que la vacuna, ofrecida en dos dosis - preparatoria y de refuerzo-, es efectiva en una media del 70,4%, aunque la variación en la cantidad de cada dosis afecta al resultado.
Cuando se administra media dosis seguida de una dosis completa, el nivel de eficacia asciende al 90% -y reduce la transmisión- y desciende al 62% cuando los voluntarios reciben dos dosis enteras del antídoto.
Tras el anuncio, se supo que las diferencias en la cantidad de las dosis administradas entre los diferentes grupos parten de una equivocación y que la dosis que obtuvo una eficacia del 90% se adjudicó a un grupo con muchos menos participantes, lo que para algunos implica cuestionar los resultados.
Explicación de la Universidad de Oxford
En su nota, la universidad explica que en su estudio "se emplearon dos niveles de dosis, basados en la misma medida de la concentración empleada en la fase I pero, como resultado de una diferencia en el proceso de manufactura para el último estudio, se demostró posteriormente que este método sobreestimó la dosis en los nuevos lotes, lo que resultó en la administración de media dosis como primera dosis".
Agrega que "cuando quedó patente que se había usado una dosis menor" se trasladó la cuestión al regulador y se acordó un plan para probar esa combinación, permitiendo al equipo investigador "incluir ambos planteamientos en la fase III del ensayo". "Los métodos para medir la concentración han quedado ya establecidos y podemos asegurar que todos los lotes de la vacuna son ahora equivalentes", concluye la nota.
Denuncia desde EEUU
Según el diario Financial Times, el responsable del programa de financiación para el desarrollo de vacunas de EEUU, Moncef Slaoui, reveló que el subgrupo -de apenas 2.300 personas- que recibió la dosis más efectiva se limitó a individuos menores de 55 años, con menor riesgo de desarrollar síntomas severos de Covid, un dato que no divulgaron ni la universidad ni AstraZeneca al presentar sus datos. Por ello, Slaoui baraja la posibilidad de que la diferencia en la eficacia de la vacuna haya sido "fortuita".
AstraZeneca planea un nuevo estudio para validar la eficacia de su vacuna
Unas horas después del comunicado de la Universidad de Oxford, la farmacéutica AstraZeneca dijo que valora realizar un "estudio adicional" que valide los resultados de la eficacia de su vacuna, según el consejero delegado de la firma, Pascal Soriot. El responsable de la farmacéutica aseguró en una entrevista con Bloomberg que no espera que esos nuevos test retrasen la aprobación de los reguladores sanitarios en el Reino Unido y la Unión Europea.
"Ahora que hemos detectado lo que parece ser una mejor eficacia -dijo sobre la confusión con las dosis-, debemos validarlo, así que necesitamos hacer un estudio adicional", afirmó Soriot. El consejero delegado detalló que se realizará probablemente un nuevo "estudio internacional", si bien aseguró que "este podría ser más rápido" que los anteriores, porque los investigadores ya saben que la eficacia de la vacuna es "alta" y necesitan "un número más reducido de pacientes".
Recalcó asimismo que la autorización para comenzar la vacunación en algunos países continúa prevista para antes de final de año, si bien en Estados Unidos el proceso se prevé más largo, dado que los ensayos se llevaron a cabo fuera de ese país.
También te puede interesar
Lo último